Сообщение о кремнии. Кремний: применение, химические и физические свойства. Сочетание с другими питательными веществами
Кремний. Физические и химические свойства кремния
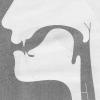
Кремний - элемент главной подгруппы четвёртой группы третьего периода периодической системы химических элементов Д.И. Менделеева, с атомным номером 14. Обозначается символом Si (лат. Silicium), неметалл. Физические свойства: кристаллический кремний обладает металлическим блеском, тугоплавкий, очень твердый, полупроводник. 2. Химические свойства: кремний малоактивен: а) при повышенных температурах (400-600
- б) из сложных веществ кремний реагирует со щелочами
- в) реагирует с металлами с образованием силицидов
Кремнезем, его свойства и применение. Природные и промышленные силикаты. Их применение в строительстве
Oксид кремния (IV) (диоксид кремния, кремнезём SiO2 ) - бесцветные кристаллы, tпл 1713--1728 °C, обладают высокой твёрдостью и прочностью.
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках. Диоксид кремния - главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента. Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов. Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов. Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали. Крупные прозрачные кристаллы кварца используются в качестве полудрагоценных камней; бесцветные кристаллы называют горным хрусталём, фиолетовые - аметистами, жёлтые - цитрином. В микроэлектронике диоксид кремния является одним из основных материалов. Его применяют в качестве изолирующего слоя, а также в качестве защитного покрытия. Получают в виде тонких плёнок термическим окислением кремния, химическим осаждением из газовой фазы, магнетронным распылением. Диоксид кремния SiO2 - кислотный оксид, не реагирующий с водой. Химически стоек к действию кислот, но реагирует с газообразным фтороводородом
и плавиковой кислотой:
Эти две реакции широко используют для травления стекла. При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты - соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xH2O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же веществе).
Например, может быть получен ортосиликат натрия:
метасиликат кальция:
или смешанный силикат кальция и натрия:
Из силиката
Na2CaSi6O14 (Na2O·CaO·6SiO2)
изготовляют оконное стекло. Большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют жидким стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот. Главным структурным элементом, как твердого диоксида кремния, так и всех силикатов, выступает группа , в которой атом кремния Si окружен тетраэдром из четырёх атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие. Силикаты - это обширный класс соединений, образованных диоксидом кремния (кремнеземом) и оксидами других элементов. СИЛИКАТЫ В ПРИРОДЕ. Для того чтобы понять роль силикатов в жизни человека, остановимся сначала на строении земного шара . По современным представлениям земной шар состоит из ряда оболочек. Наружная оболочка Земли, земная кора, или литосфера, образована гранитной и базальтовой оболочками и тонким осадочным слоем. Гранитная оболочка в основном состоит из гранита - плотных сростков из полевых шпатов, слюды, амфиболов и пироксенов, а базальтовая - из таких гранитоподобных, но более тяжелых силикатных пород, как габбро, диабазы и базальты. Осадочные горные породы образуются при разрушении других пород под влиянием условий, характерных для поверхности Земли. Составной частью осадочного слоя являются, в частности, глины, основа которых - силикатный минерал каолинит. Литосфера на 95 мас. % образована силикатами. Ее средняя мощность в области материков составляет 30-40 км. Затем располагается симатическая оболочка, или верхняя мантия, среди минералов которой, вероятно, преобладают силикаты железа и магния. Эта оболочка охватывает земной шар сплошь и распространяется до глубины 1200 км. Далее от 1200 до 2900 км располагается промежуточная оболочка. Ее состав спорен, но и в ней предполагается существование силикатов. Под этой оболочкой на глубине от 2900 до 6370 км находится ядро. В последнее время высказано предположение, что ядро имеет также силикатный состав. При движении от поверхности Земли к ее центру возрастают плотность и основность слагающих пород (увеличивается соотношение между содержанием оксидов металлов и кремнезема), давление и температура. Древнейшие орудия труда были изготовлены человеком из кремня - плотного агрегата из халцедона, кварца и опала (800-60 тыс. лет до н.э.). Позднее для этого стали использовать яшмы, горный хрусталь, агаты, обсидиан (вулканическое силикатное стекло), нефрит.ля силикатных минералов нет общепринятой систематики (минералогической номенклатуры), их названия чаще всего происходят от внешнего вида кристаллов, их физических свойств, места нахождения или имени ученого, их открывшего. Плагиоклаз в переводе с греческого означает косо раскалывающийся, а пироксен - тугоплавкий, что отвечает свойствам этих минералов. Минералы кварца в зависимости от природы примесей имеют широкий спектр окраски, которая и определяет их названия: аметист - фиолетовый, цитрин - желтый, горный хрусталь - лед. Модификации кремнезема стишовита и коэсита и минерала биотита произошли от фамилий ученых, их открывших, С.М. Стишова, Л. Коэса и Ж.Б. Био, а минерал каолинит получил свое название от горы Каолинг в Китае, где издавна добывалась глина для производства фарфора. Природные силикаты и сам кремнезем играют важную роль в качестве сырья и конечных продуктов в промышленных процессах. Алюмосиликаты - плагиоклазы, калиевый полевой шпат и кремнезем используются как сырье в керамической, стекольной и цементной промышленности. Для изготовления несгораемых и обладающих электроизоляционными свойствами текстильных изделий (ткани, шнуры, канаты) широко используются асбесты, относящиеся к гидросиликатам - амфиболам. Некоторые виды асбестов обладают высокой кислотостойкостью и применяются в химической промышленности. Биотиты, представители группы слюд, используются как электро- и теплоизоляционные материалы в строительстве и приборостроении. Пироксены применяются в металлургии и каменно-литейном производстве, а пироксен LiAl - для получения металлического лития. Пироксены являются составной частью доменных шлаков и шлаков цветной металлургии, которые, в свою очередь, также используются в народном хозяйстве. Такие горные породы, как граниты, базальты, габбро, диабазы, являются прекрасными строительными материалами. СИЛИКАТЫ ИСКУССТВЕННОГО ПРОИСХОЖДЕНИЯ. Без силикатных материалов - различных видов цемента, бетона, шлакобетона, керамики, стекла, покрытий в виде эмалей и глазурей едва ли можно представить себе нашу повседневную жизнь. Масштабы производства силикатных материалов представляются внушительными цифрами. В статье мы не будем касаться природы и применения стекол. Эти вопросы уже были рассмотрены в .Наиболее древними силикатными материалами являются керамические, получаемые из глин и их смесей с различными минеральными добавками, обожженными до камневидного состояния. В древнем мире керамические изделия были распространены по всей территории Земли. Со второй половины XIX века и до настоящего времени индустриальная керамическая промышленность неизмеримо расширила выпуск и ассортимент керамики. Примером искусственного силикатного материала является портландцемент, один из наиболее распространенных видов минеральных вяжущих веществ. Цемент используется для связывания строительных деталей при получении массивных строительных блоков, плит, труб и кирпича. Цемент является основой таких широко применяемых строительных материалов, как бетон, шлакобетон, железобетон. Строительство любого масштаба не может существовать без цемента. В школьном курсе по химии даны основные представления о химическом составе и технологии цемента, поэтому остановимся лишь на некоторых уточняющих деталях. Прежде всего, цементным клинкером называется продукт обжига смеси глины и известняка, а цементом - мелкоизмельченный клинкер с минеральными добавками, регулирующими его свойства. Цемент применяется в смеси с песком и водой. Его вяжущие свойства обусловлены способностью цементных минералов взаимодействовать с H2O и SiO2 и при этом затвердевать, образуя прочную камневидную структуру. При схватывании цемента происходят сложные процессы: гидратация минералов с образованием гидросиликатов и гидроалюминатов, гидролиз, образование коллоидных растворов и их кристаллизация. Исследования процессов твердения цементного раствора и минералов цементного клинкера сыграли большую роль в становлении науки о силикатах и их технологии. Наши стройки в больших количествах потребляют цемент, кирпич, облицовочные плиты, черепицу, канализационные трубы, стекло и различные природные строительные материалы.
Кремний - химический элемент IV группы Периодической системы элементов Д.И. Менделеева. Открыт в 1811 г. Ж. Гей-Люсаком и Л. Тернаром. Его порядковый номер 14, атомная масса 28,08, атомный объем 12,04 10 -6 м 3 /моль. Кремний - металлоид, принадлежит к подгруппе углерода. Его валентность по кислороду +2 и +4. По распространенности в природе кремний уступает только кислороду. Его массовая доля в земной коре составляет 27,6 %. Земная кора, по мнению В.И. Вернадского, более чем на 97 % состоит из кремнезема и силикатов. Кислородные и органические соединения кремния входят также в состав растений и животных.
Искусственно полученный кремнии может быть как аморфным, так и кристаллическим. Аморфный кремний - коричневый, тонко дисперсный, сильно гигроскопичный порошок, по рентгеноструктурным данным, состоит из мельчайших кристалликов кремния. Он может быть получен восстановлением при высоких температурах SiCl 4 парами цинка.
Кристаллический кремний имеет серо-стальной цвет и отличается металлическим блеском. Плотность кристаллического кремния при 20°С составляет 2,33 г/см 3 , жидкого кремния при 1723-2,51, а при 1903К — 2,445 г/см 3 . Температура плавления кремния - 1690 К, кипения - 3513 К. В соответствии с данными, давление паров кремния при Т = 2500÷4000 К описывается уравнением lg p Si = -20130/ Т + 7,736, кПа. Теплота возгонки кремния 452610, плавления 49790, испарения 385020 Дж/моль.
Поликристаллы кремния отличаются высокой твердостью (при 20°С HRC = 106). Однако кремний очень хрупок, поэтому имеет высокую прочность при сжатии (σ СЖ В ≈690 МПа) и очень низкое сопротивление разрыву (σ В ≈ 16,7 МПа).
При комнатной температуре кремний инертен, реагирует только со фтором, образуя летучий 81Р4. Из кислот реагирует только с азотной в смеси с плавиковой кислотой. Со щелочами, однако, кремний реагирует довольно легко. Одна из его реакции со щелочами
Si + NaOH + H 2 O = Na 2 SiO 3 + 2H 2
используется для получения водорода. Вместе с этим с неметаллами кремний способен давать большое количество химически прочных соединений. Из подобных соединений необходимо отметить галогениды (от SiX 4 до Si n X 2n+2 , где X - галоген, а n ≤ 25), их смешанные соединения SiCl 3 B, SiFCl 3 и др., оксихлориды Si 2 OCl 3 , Si 3 O 2 Cl 3 и др., нитриды Si 3 N 4 , Si 2 N 3 , SiN и гидриды с общей формулой Si n H 2n+2 , а из соединений, встречающихся при производстве ферросплавов, - летучие сульфиды SiS и SiS 2 и тугоплавкий карбид SiC.
Кремний способен также давать соединения с металлами - силициды, наиболее важными из них являются силициды железа, хрома, марганца, молибдена, циркония, а также РЗМ и ЩЗМ. Это свойство кремния - способность давать химически очень прочные соединения и растворы с металлами - широко используется в технике производства низкоуглеродистых ферросплавов, а также при восстановлении легкокипящих щелочноземельных (Са, Mg, Ва) и трудновосстановимых металлов (Zr, Al и др.).
Сплавы кремния с железом изучены П.В. Гельдом и его школой, особое внимание было обращено на часть системы Fe-Si, относящуюся к сплавам с его высоким содержанием. Это связано с тем, что, как видно из диаграммы Fe-Si (рисунок 1), в сплавах этого состава происходит целый ряд превращений, значительно влияющих на качество ферросилиция различных марок. Так, дисилицид FeSi 2 стабилен только при низких температурах (< 918 или 968 °С, см. рисунок 1). При высоких температурах устойчива его высокотемпературная модификация - лебоит. Содержание кремния в этой фазе колеблется в пределах 53-56 %. В дальнейшем лебоит будем обозначать химической формулой Fe 2 Si 5 , что практически соответствует максимальной концентрации кремния в лебоите.
При охлаждении сплавов с содержанием > 55,5 % Si лебоит при Т < 1213 К разлагается по эвтектоидной реакции
Fe 2 Si 5 → FeSi 2 +Si (2)
а сплавов 33,86-50,07 % Si при Т < 1255 К - по перитектоидной реакции
Fe 2 Si 5 + FeSi = ЗFeSi 2 (3)
Cплавы промежуточного состава (50,15-55,5 % Si) сначала при 1255 К претерпевают перитектоидное (3), а затем при 1213 К - эвтектоидное (2) превращения. Эти превращения Fe 2 Si 5 по реакциям (2) и (3) сопровождаются изменениями объема силицида. Особенно велико подобное изменение в ходе реакции (2) - примерно 14 %, поэтому сплавы, содержащие лебоит, теряют сплошность, растрескиваются и даже рассыпаются. При медленной, равновесной кристаллизации (см. рисунок 1) лебоит может выделяться при кристаллизации как сплава ФС75, так и ФС45.
Однако растрескивание, связанное с эвтектоидным распадом лебоита, лишь одна из причин рассыпания. Второй причиной, по-видимому главной, является то, что образование трещин по границам зерна создает возможность ликватам, выделяющимся по этим границам - фосфору, мышьяку, сульфидам и карбидам алюминия и др., - реагировать с влагой воздуха по реакциям, в результате которых в атмосферу выделяются H 2 , PH 3 , PH 4 , AsH 4 и т.п., а в трещинах — рыхлые оксиды Al 2 O 3 , SiO 2 и другие соединения, распирающие их. Предотвратить рассыпание сплавов можно их модифицированием магнием, легированием добавками элементов, измельчающих зерно (V, Ti, Zг и др.) или делающих его более пластичным. Измельчение зерна уменьшает на его границах концентрацию примесей и их соединений и влияет на свойства сплавов так же, как общее понижение в сплаве концентрации примесей (P, Al, Ca), способствующих рассыпанию. Термодинамические свойства сплавов Fe-Si (теплота смешения, активность, растворимость углерода) изучены подробно, их можно найти в работах. Сведения о растворимости углерода в сплавах Fe-Si приведены на рисунке 2, об активности кремния - в таблице 1.
Рисунок 1. — Диаграмма состояния системы Fe-Si


Физико-химические свойства кислородных соединений кремния изучал П.В. Гельд с сотрудниками. Несмотря на важность системы Si-O, ее диаграмма до сих пор не построена. В настоящее время известны два кислородных соединения кремния - кремнезем SiO 2 и монооксид SiO. В литературе имеются также указания о существовании и других кислородных соединений кремния - Si 2 O 3 и Si 3 O 4 , однако сведения об их химических и физических свойствах отсутствуют.
В природе кремний представлен только кремнеземом SiO 2 . Это соединение кремния отличается:
1) высокой твердостью (по шкале Мооса 7) и тугоплавкостью (T пл = 1996 К);
2) высокой температурой кипения (Т КИП = 3532 К). Давление паров кремнезема может бьггь описано уравнениями (Па):
3) образованием большого количества модификаций:
 Особенностью аллотропных превращений SiO 2 является то, что они сопровождаются значительными изменениями плотности и объема вещества, что может вызвать растрескивание и измельчение породы;
Особенностью аллотропных превращений SiO 2 является то, что они сопровождаются значительными изменениями плотности и объема вещества, что может вызвать растрескивание и измельчение породы;
4) высокой склонностью к переохлаждению. Поэтому имеется возможность в результате быстрого охлаждения зафиксировать структуру как жидкого расплава (стекло), так и высокотемпературных модификаций в-кристобалита и тридимита. Наоборот, при быстром нагревании можно расплавить кварц, минуя структуры тридимита и кристобалита. Температура плавления SiO 2 при этом понижается примерно на 100 °С;
5) высоким электросопротивлением. Например, при 293 К оно составляет 1 10 12 Ом*м. Однако с повышением температуры электросопротивление SiO 2 понижается, а в жидком состоянии кремнезем — неплохой проводник;
6) высокой вязкостью. Так, при 2073 К вязкость равна 1 10 4 Па с, а при 2273 К - 280 Па с.
Последнее, по мнению Н.В. Соломина, объясняется тем, что SiO 2 , подобно органическим полимерам, способен образовывать цепочки, которые при 2073 К состоят из 700, а при 2273 К — из 590 молекул SiO 2 ;
7) высокой термической устойчивостью. Энергия Гиббса образования SiO 2 из элементов с учетом агрегатного их состояния в соответствии с данными с высокой точностью описывается уравнениями:
Эти данные, как видно из таблицы 2, несколько отличаются от данных авторов. Для термодинамических расчетов могут использоваться и двухчленные уравнения:

Монооксид кремния SiO обнаружен в 1895 г. Поттером в газовой фазе электропечей. В настоящее время надежно установлено, что SiO существует и в конденсированных фазах. По исследованиям П.В. Гельда, оксид отличается невысокой плотностью (2,15 г/см 3), высоким электросопротивлением (10 5 -10 6 Ом*м). Конденсированный оксид хрупок, его твердость по шкале Мооса ∼ 5. Температуру плавления вследствие высокой его летучести экспериментально определить не удалось. По данным О. Кубашевского, она равна 1875 К, по мнению Бережного, - 1883 К. Теплота плавления SiO в несколько раз выше ΔH 0 SiO2 по данным она равна 50242 Дж/моль. По-видимому, вследствие летучести она завышена. Имеет стекловидный излом, его цвет изменяется от белого до шоколадного, что связано, вероятно, с его окислением кислородом воздуха. Свежий излом SiO обычно имеет гороховатый цвет с жирным блеском. Термодинамически стабилен оксид только при высоких температурах в виде SiO (Г) . При охлаждении оксид диспропорционирует по реакции
2SiO (Г) = SiO (Ж) + SiO 2 (6)

Температуру кипения SiO можно ориентировочно оценить из уравнения:
Газообразный оксид кремния термодинамически очень стоек. Энергию Гиббса его образования можно описать уравнениями (см. таблицу 2):

из которых видно, что химическая прочность SiO подобно CO с ростом температуры повышается, что делает его прекрасным восстановителем для многих веществ.
Для термодинамического анализа можно использовать и двухчленные уравнения:
 Состав газов над SiO 2 оценивался И.С. Куликовым. В зависимости от температуры содержание SiO над SiO 2 описывается уравнениями:
Состав газов над SiO 2 оценивался И.С. Куликовым. В зависимости от температуры содержание SiO над SiO 2 описывается уравнениями:
Карбид кремния, как и SiO, является одним из промежуточных соединений, образующихся в ходе восстановления SiO 2 . Карбид отличается высокой температурой плавления.
В зависимости от давления он стоек вплоть до 3033-3103 К (рисунок 3). При высоких температурах карбид кремния сублимирует. Однако давление паров Si (Г) , Si 2 C (Г) , SiC 2(Г) над карбидом при Т < 2800К невелико, что следует из уравнения
Карбид существует в виде двух модификаций - кубической низкотемпературной β-SiC и гексагональной высокотемпературной α-SiC. В ферросплавных печах обычно встречается лишь β-SiC. Как показали расчеты с использованием данных, энергия Гиббса образования описывается уравнениями:

которые заметно отличаются от данных. Из этих уравнений следует, что карбид термически стоек до 3194 К. По физическим свойствам карбид отличается высокой твердостью (~ 10), высоким электросопротивлением (при 1273К p≈0,13 ⋅ 10 4 мкОм ⋅ м), повышенной плотностью (3,22 г/см 3) и высокой стойкостью как в восстановительной, так и в окислительной атмосфере.
По внешнему виду чистый карбид бесцветен, обладает полупроводниковыми свойствами, которые сохраняются и при высоких температурах. Технический карбид кремния содержит примеси и поэтому окрашен в зеленый или черный цвет. Так, зеленый карбид содержит 0,5-1,3 % примесей (0,1-0,3 % C, 0,2-1,2 % Si + SiO 2 , 0,05-0,20 % Fe 2 O 3 , 0,01- 0,08 % Al 2 O 3 и др.). В черном карбиде содержание примесей более высокое (1-2 %).
В качестве восстановителя при производстве сплавов кремния применяют углерод. Он же является основным веществом, из которого изготавливают электроды и футеровки электропечей, выплавляющих кремний и его сплавы. Углерод довольно распространен в природе, его содержание в земной коре составляет 0,14 %. В природе он встречается как в свободном состоянии, так и в виде органических и неорганических соединений (в основном карбонатов).
Углерод (графит) имеет гексагональную кубическую решетку. Рентгеновская плотность графита 2,666 г/см 3 , пикнометрическая — 2,253 г/см 3 . Он отличается высокими температурами плавления (~ 4000 °С) и кипения (~ 4200 °С), повышающимся с ростом температуры электросопротивлением (при 873 К p≈9,6 мкОм⋅м, при 2273 К p≈ 15,0 мкОм⋅м), довольно прочен. Его временное сопротивление на усах может составить 480-500 МПа. Однако электродный графит имеет σ в = 3,4÷17,2 МПа. Твердость графита по шкале Мооса ~ 1.
Углерод - прекрасный восстановитель. Это связано с тем, что прочность одного из его кислородных соединений (СО) повышается с ростом температуры. Это видно из энергии Гиббса его образования, которая, как показали наши расчеты с использованием данных, хорошо описывается как трехчленным
так и двухчленными уравнениями:

Диоксид углерода СO 2 термодинамически прочен лишь до 1300 К. Энергия Гиббса образования CO 2 описывается уравнениями:

Содержание статьи
КРЕМНИЙ, Si (silicium), химический элемент IVA подгруппы (C, Si, Ge, Sn и Pb) периодической системы элементов, неметалл. Кремний в свободном виде был выделен в 1811 Ж.Гей-Люссаком и Л.Тенаром при пропускании паров фторида кремния над металлическим калием, однако он не был описан ими как элемент. Шведский химик Й.Берцелиус в 1823 дал описание кремния, полученного им при обработке калиевой соли K 2 SiF 6 металлическим калием при высокой температуре, однако лишь в 1854 кремний был получен в кристаллической форме А.Девилем. Кремний – второй по распространенности (после кислорода) элемент в земной коре, где он составляет более 25% (масс.). Встречается в природе в основном в виде песка, или кремнезема, который представляет собой диоксид кремния, и в виде силикатов (полевые шпаты M (M = Na, K, Ba), каолинит Al 4 (OH) 8 , слюды). Кремний можно получить прокаливанием измельченного песка с алюминием или магнием; в последнем случае его отделяют от образующегося MgO растворением оксида магния в соляной кислоте. Технический кремний получают в больших количествах в электрических печах путем восстановления кремнезема углем или коксом. Полупроводниковый кремний получают восстановлением SiCl 4 или SiHCl 3 водородом с последующим разложением образующегося SiH 4 при 400–600° С. Высокочистый кремний получают выращиванием монокристалла из расплава полупроводникового кремния по методу Чохральского или методом бестигельной зонной плавки кремниевых стержней . Элементный кремний получают в основном для полупроводниковой техники, в остальных случаях он используется как легирующая добавка в производстве сталей и сплавов цветных металлов (например, для получения ферросилиция FeSi, который образуется при прокаливании смеси песка, кокса и оксида железа в электрической печи и применяется как раскислитель и легирующая добавка в производстве сталей и как восстановитель в производстве ферросплавов).
Применение.
Наибольшее применение кремний находит в производстве сплавов для придания прочности алюминию, меди и магнию и для получения ферросилицидов, имеющих важное значение в производстве сталей и полупроводниковой техники. Кристаллы кремния применяют в солнечных батареях и полупроводниковых устройствах – транзисторах и диодах. Кремний служит также сырьем для производства кремнийорганических соединений, или силоксанов, получаемых в виде масел, смазок, пластмасс и синтетических каучуков. Неорганические соединения кремния используют в технологии керамики и стекла, как изоляционный материал и пьезокристаллы.
|
СВОЙСТВА КРЕМНИЯ |
|
| Атомный номер | 14 |
| Атомная масса | 28,086 |
| Изотопы | |
| стабильные | 28, 29, 30 |
| нестабильные | 25, 26, 27, 31, 32, 33 |
| Температура плавления, °С | 1410 |
| Температура кипения, °С | 2355 |
| Плотность, г/см 3 | 2,33 |
| Твердость (по Моосу) | 7,0 |
| Содержание в земной коре, % (масс.) | 27,72 |
| Степени окисления | –4, +2, +4 |
Свойства.
Кремний – темносерое, блестящее кристаллическое вещество, хрупкое и очень твердое, кристаллизуется в решетке алмаза. Это типичный полупроводник (проводит электричество лучше, чем изолятор типа каучука, и хуже проводника – меди). При высокой температуре кремний весьма реакционноспособен и взаимодействует с большинством элементов, образуя силициды, например силицид магния Mg 2 Si, и другие соединения, например SiO 2 (диоксид кремния), SiF 4 (тетрафторид кремния) и SiC (карбид кремния, карборунд). Кремний растворяется в горячем растворе щелочи с выделением водорода: Si + NaOH ® Na 4 SiO 4 + 2H 2 . 4 (тетрахлорид кремния) получают из SiO 2 и CCl 4 при высокой температуре; это бесцветная жидкость, кипящая при 58° С, легко гидролизуется, образуя хлороводородную (соляную) кислоту HCl и ортокремниевую кислоту H 4 SiO 4 (это свойство используют для создания дымовых надписей: выделяющаяся HCl в присутствии аммиака образует белое облако хлорида аммония NH 4 Cl). Тетрафторид кремния SiF 4 образуется при действии фтороводородной (плавиковой) кислоты на стекло:
Na 2 SiO 3 + 6HF ® 2NaF + SiF 4 + 3H 2 O
SiF 4 гидролизуется, образуя ортокремниевую и гексафторокремниевую (H 2 SiF 6) кислоты. H 2 SiF 6 по силе близка к серной кислоте. Многие фторосиликаты металлов растворимы в воде (соли натрия, бария, калия, рубидия, цезия малорастворимы), поэтому HF используют для перевода минералов в раствор при выполнении анализов. Сама кислота H 2 SiF 6 и ее соли ядовиты.
Кремниевые кислоты.
Две оксокислоты кремния H 4 SiO 4 (ортокремниевая) и H 2 SiO 3 (метакремниевая, или кремниевая) существуют только в растворе и необратимо превращаются в SiO 2 , если выпарить воду. Другие кремниевые кислоты получаются за счет различного количества воды в их составе: H 6 Si 2 O 7 (пирокремниевая кислота из двух молекул ортокремниевой кислоты), H 2 Si 2 O 5 и H 4 Si 3 O 8 (ди- и трикремниевая кислоты из двух и соответственно трех молекул метакремниевой кислоты). Все кислоты кремния слабые. При добавлении в раствор силиката серной кислоты образуется гель (желатинообразное вещество), при нагревании и высушивании которого остается твердый пористый продукт – силикагель, имеющий развитую поверхность и используемый как адсорбент газов, осушитель, катализатор и носитель катализаторов.
После кислорода кремний является самым распространенным элементом в земной коре. Он имеет 2 устойчивых изотопа: 28 Si , 29 Si , 30 Si . В свободном виде кремний в природе не встречается.
Наиболее часто встречающиеся: соли кремниевых кислот и оксид кремний (кремнезем, песок, кварц). Они входят в состав минеральных солей, слюды, талька, асбеста.
Аллотропия кремния.
У кремния есть 2 аллотропные модификации:
Кристаллическая (светло-серые кристаллы. Структура подобна кристаллической решетке алмаза, где атом кремния ковалентно связан с 4 одинаковыми атомами , а сам находится в sp 3 - гибридизации);
Аморфная (порошок бурого цвета, более активная форма чем кристаллическая).
Свойства кремния.
При температуре кремний реагируют с кислородом воздуха:
Si + O 2 = SiO 2 .
Если кислорода не хватает (недостаток), то может иметь место такая реакция:
2 Si + O 2 = 2 SiO ,
Где SiO - монооксид, который также может образовываться при реакции:
Si + SiO 2 = 2 SiO .
В нормальных условиях кремний может реагировать с F 2 , при нагревании - с Cl 2 . Если повышать температуру дальше, то Si будет способен провзаимодействовать с N и S :
4Si + S 8 = 4SiS 2 ;
Si + 2F 2 = SiF 4 .
Кремний способен реагировать с углеродом , давая карборунд :
Si + C = SiC .
Кремний растворим в смеси концентрированной азотной и фтороводородной кислот:
3Si + 4HNO 3 + 12HF = 3SiF 4 + 4NO + 8H 2 O.
Кремний растворяется в водных растворах щелочей:
Si + 2NaOH + H 2 O = Na 2 SiO 3 + H 2 .
При нагревании с оксидами кремний диспропорционирует:
2 MgO + 3 Si = Mg 2 Si + 2 SiO .
При взаимодействии с металлами, кремний выступает в качестве окислителя:
2 Mg + Si = Mg 2 Si .
Применение кремния.
Наибольшее применение кремний находит в производстве сплавов для придания прочности алюминию, меди и магнию и для получения ферросилицидов, имеющих важное значение в производстве сталей и полупроводниковой техники. Кристаллы кремния применяют в солнечных батареях и полупроводниковых устройствах - транзисторах и диодах.
Кремний служит также сырьем для производства кремнийорганических соединений, или силоксанов, получаемых в виде масел, смазок, пластмасс и синтетических каучуков. Неорганические соединения кремния используют в технологии керамики и стекла, как изоляционный материал и пьезокристаллы.
Один из самых распространенных в природе элементов - это silicium, или кремний. Такое широкое расселение говорит о важности и значимости данного вещества. Это быстро поняли и усвоили люди, которые научились правильно использовать в своих целях кремний. Применение его основано на особых свойствах, о которых и поговорим дальше.
Кремний - химический элемент
Если давать характеристику данного элемента по положению в периодической системе, то можно обозначить следующие важные пункты:
- Порядковый номер - 14.
- Период - третий малый.
- Группа - IV.
- Подгруппа - главная.
- Строение внешней электронной оболочки выражается формулой 3s 2 3p 2 .
- Элемент кремний обозначается химическим символом Si, который произносится как "силициум".
- Степени окисления, которые он проявляет: -4; +2; +4.
- Валентность атома равна IV.
- Атомная масса кремния равна 28,086.
- В природе существует три устойчивых изотопа данного элемента с массовыми числами 28, 29 и 30.
Таким образом, атом кремния с химической точки зрения - достаточно изученный элемент, описано множество различных его свойств.
История открытия
Так как в природе очень популярны и массовы по содержанию именно различные соединения рассматриваемого элемента, издревле люди использовали и знали о свойствах именно многих из них. Чистый же кремний долгое время оставался за гранью познаний человека в химии.
Наиболее популярными соединениями, которыми пользовались в быту и промышленности народы древних культур (египтяне, римляне, китайцы, русичи, персы и прочие), были драгоценные и поделочные камни на основе оксида кремния. К ним относятся:
- опал;
- горный хрусталь;
- топаз;
- хризопраз;
- оникс;
- халцедон и другие.
Также издревле принято использовать кварц и в строительном деле. Однако сам элементарный кремний оставался нераскрытым вплоть до XIX века, хотя многие ученые тщетно пытались выделить его из разных соединений, используя для этого и катализаторы, и высокие температуры, и даже электрический ток. Это такие светлые умы, как:
- Карл Шееле;
- Гей-Люссак;
- Тенар;
- Гемфри Дэви;
- Антуан Лавуазье.
Осуществить удачно получение кремния в чистом виде удалось Йенсу Якобсу Берцелиусу в 1823 году. Для этого он проводил опыт по сплавлению паров фтористого кремния и металлического калия. В результате получил аморфную модификацию рассматриваемого элемента. Этим же ученым было предложено латинское название открытому атому.

Еще несколько позже, в 1855 году, другой ученый - Сент Клер-Девилль - сумел синтезировать другую аллотропную разновидность - кристаллический кремний. С тех пор знания о данном элементе и его свойствах стали очень быстро пополняться. Люди поняли, что он обладает уникальными особенностями, которые можно очень грамотно использовать для удовлетворения собственных нужд. Поэтому сегодня один из самых востребованных элементов в электронике и технике - это кремний. Применение его лишь расширяет свои границы с каждым годом.
Русское название атому дал ученый Гесс в 1831 году. Именно оно и закрепилось до сегодняшнего дня.
По распространенности в природе кремний занимает второе место после кислорода. Его процентное соотношение в сравнении с другими атомами в составе земной коры - 29,5%. Кроме того, углерод и кремний - это два особых элемента, способных формировать цепи, соединяясь друг с другом. Именно поэтому для последнего известно более 400 различных природных минералов, в составе которых он и содержится в литосфере, гидросфере и биомассе.
Где конкретно содержится кремний?
- В глубоких слоях почвы.
- В горных породах, залежах и массивах.
- На дне водоемов, особенно морей и океанов.
- В растениях и морских обитателях царства животных.
- В организме человека и наземных животных.
Можно обозначить несколько самых распространенных минералов и горных пород, в составе которых в большом количестве присутствует кремний. Химия их такова, что массовое содержание чистого элемента в них достигает 75%. Однако конкретная цифра зависит от разновидности материала. Итак, горные породы и минералы с содержанием кремния:
- полевые шпаты;
- слюды;
- амфиболы;
- опалы;
- халцедоны;
- силикаты;
- песчаники;
- алюмосиликаты;
- глины и прочие.
Накапливаясь в панцирях и наружных скелетах морских животных, кремний со временем формирует мощные залежи кремнезема на дне водоемов. Это один из природных источников данного элемента.
Кроме того, было установлено, что силициум может существовать в чистом самородном виде - в виде кристаллов. Но подобные месторождения очень редки.

Физические свойства кремния
Если давать характеристику рассматриваемого элемента по набору физико-химических свойств, то в первую очередь следует обозначить именно физические параметры. Вот несколько основных:
- Существует в виде двух аллотропных модификаций - аморфный и кристаллический, которые отличаются по всем свойствам.
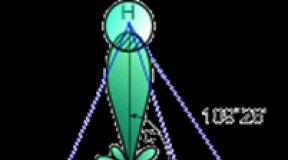
- Кристаллическая решетка очень схожа с таковой у алмаза, ведь углерод и кремний в этом отношении практически одинаковы. Однако расстояние между атомами разное (у кремния больше), поэтому алмаз гораздо тверже и прочнее. Тип решетки - кубическая гранецентрированная.
- Вещество очень хрупкое, при высоких температурах становится пластичным.
- Температура плавления равна 1415˚С.
- Температура кипения - 3250˚С.
- Плотность вещества - 2,33 г/см 3 .
- Цвет соединения - серебристо-серый, выражен характерный металлический блеск.
- Обладает хорошими полупроводниковыми свойствами, которые способны варьировать при добавлении тех или иных агентов.
- Не растворяется в воде, органических растворителях и кислотах.
- Специфически растворим в щелочах.
Обозначенные физические свойства кремния позволяют людям управлять им и применять для создания различных изделий. Так, например, на свойствах полупроводимости основано использование чистого кремния в электронике.
Химические свойства
Химические свойства кремния очень сильно зависят от условий проведения реакции. Если говорить о при стандартных параметрах, то нужно обозначить очень низкую активность. Как кристаллический, так и аморфный кремний очень инертны. Не взаимодействуют ни с сильными окислителями (кроме фтора), ни с сильными восстановителями.
Это связано с тем, что на поверхности вещества мгновенно формируется оксидная пленка SiO 2 , которая препятствует дальнейшим взаимодействиям. Она способна образоваться под влиянием воды, воздуха, паров.
Если же изменить стандартные условия и произвести нагревание кремния до температуры свыше 400˚С, то его химическая активность сильно возрастет. В этом случае он будет вступать в реакции с:
- кислородом;
- всеми видами галогенов;
- водородом.
При дальнейшем повышении температуры возможно образование продуктов при взаимодействии с бором, азотом и углеродом. Особое значение имеет карборунд - SiC, так как он является хорошим абразивным материалом.
Также химические свойства кремния четко прослеживаются при реакциях с металлами. По отношению к ним он окислитель, поэтому продукты носят название силицидов. Известны подобные соединения для:
- щелочных;
- щелочноземельных;
- переходных металлов.
Необычными свойствами обладает соединение, получаемое при сплавлении железа и кремния. Оно носит название ферросилициевой керамики и успешно применяется в промышленности.
Со сложными веществами кремний во взаимодействие не вступает, поэтому из всех их разновидностей способен растворяться лишь в:
- царской водке (смесь азотной и соляной кислот);
- едких щелочах.
При этом температура раствора должна быть не меньше 60˚С. Все это еще раз подтверждает физическую основу вещества - алмазоподобную устойчивую кристаллическую решетку, придающую ему прочность и инертность.

Способы получения
Получение кремния в чистом виде - процесс достаточно затратный экономически. Кроме того, в силу его свойств любой способ дает лишь на 90-99 % чистый продукт, в то время как примеси в виде металлов и углерода остаются все равно. Поэтому просто получить вещество недостаточно. Его следует еще и качественно очистить от посторонних элементов.
В целом же производство кремния осуществляется двумя основными путями:
- Из белого песка, который представляет собой чистый оксид кремния SiO 2 . При прокаливании его с активными металлами (чаще всего с магнием) происходит образование свободного элемента в виде аморфной модификации. Чистота такого способа высока, продукт получается с 99,9-процентным выходом.
- Более широко распространенный способ в промышленных масштабах - это спекание расплава песка с коксом в специализированных термических печах для обжига. Данный способ был разработан русским ученым Бекетовым Н. Н.
Дальнейшая обработка заключается в подвергании продуктов методам очистки. Для этого используются кислоты или галогены (хлор, фтор).
Аморфный кремний
Характеристика кремния будет неполной, если не рассмотреть отдельно каждую его аллотропную модификацию. Первая из них - это аморфная. В таком состоянии рассматриваемое нами вещество представляет собой порошок буро-коричневого цвета, мелкодисперсный. Обладает высокой степенью гигроскопичности, проявляет достаточно высокую химическую активность при нагревании. В стандартных условиях способен взаимодействовать только с сильнейшим окислителем - фтором.
Называть аморфный кремний именно разновидностью кристаллического не совсем правильно. Его решетка показывает, что данное вещество - это лишь форма мелкодисперсного кремния, существующего в виде кристаллов. Поэтому как таковые эти модификации - одно и то же соединение.

Однако свойства их различаются, поэтому и принято говорить об аллотропии. Сам по себе аморфный кремний обладает высокой светопоглотительной способностью. Кроме того, при определенных условиях данный показатель в разы превышает подобный у кристаллической формы. Поэтому его используют в технических целях. В рассматриваемом виде (порошок) соединение легко наносится на любую поверхность, будь то пластик или стекло. Поэтому так удобен для использования именно аморфный кремний. Применение основано на различных размеров.
Хотя износ батарей подобного типа довольно быстрый, что связано с истиранием тонкой пленки вещества, однако применение и востребованность только растет. Ведь даже за короткий срок службы солнечные батареи на основе аморфного кремния способны обеспечить энергией целые предприятия. К тому же производство подобного вещества безотходное, что делает его очень экономным.
Получают такую модификацию путем восстановления соединений активными металлами, например, натрием или магнием.

Кристаллический кремний
Серебристо-серая блестящая модификация рассматриваемого элемента. Именно такая форма является самой распространенной и наиболее востребованной. Это объясняется набором качественных свойств, которыми обладает данное вещество.
Характеристика кремния с кристаллической решеткой включает в себя классификацию его видов, так как их несколько:
- Электронного качества - самый чистый и максимально высококачественный. Именно такой вид используется в электронике для создания особо чувствительных приборов.
- Солнечного качества. Само название определяет область использования. Это также достаточно высокий по чистоте кремний, применение которого необходимо для создания качественных и долго работающих солнечных батарей. Фотоэлектрические преобразователи, созданные на основе именно кристаллической структуры, более качественны и износостойки, нежели те, что созданы с использованием аморфной модификации путем напыления на различного типа подложки.
- Технический кремний. В данную разновидность включаются те образцы вещества, в которых содержится около 98 % чистого элемента. Все остальное уходит на различного рода примеси:
- алюминий;
- хлор;
- углерод;
- фосфор и прочие.
Последняя разновидность рассматриваемого вещества используется с целью получения поликристаллов кремния. Для этого проводятся процессы перекристаллизации. Вследствие этого по чистоте получаются такие продукты, которые можно относить к группам солнечного и электронного качества.
По своей природе поликремний - это промежуточный продукт между аморфной модификацией и кристаллической. С таким вариантом легче работать, он лучше подвергается переработке и очистке фтором и хлором.
Продукты, которые получаются в результате, можно классифицировать так:
- мультикремний;
- монокристаллический;
- профилированные кристаллы;
- кремниевый скрап;
- технический кремний;
- отходы производства в виде осколков и обрезков вещества.
Каждый из них находит применение в промышленности и используется человеком полностью. Поэтому касающиеся кремния, считаются безотходными. Это значительно снижает его экономическую стоимость, при этом не влияя на качество.

Использование чистого кремния
Производство кремния в промышленности налажено достаточно хорошо, а его масштабы довольно объемны. Это связано с тем, что данный элемент, как чистый, так и в виде различных соединений, широко распространен и востребован в разных отраслях науки и техники.
Где же используется кристаллический и аморфный кремний в чистом виде?
- В металлургии как легирующая добавка, способная менять свойства металлов и их сплавов. Так, он используется при выплавке стали и чугуна.
- Разные виды вещества уходят на изготовление более чистого варианта - поликремния.
- Соединения кремния с - это целая химическая отрасль, которая получила особую популярность сегодня. Кремнийорганические материалы используются в медицине, при изготовлении посуды, инструментов и многого другого.
- Изготовление различных солнечных батарей. Этот способ получения энергии является одним из самых перспективных в будущем. Экологически чисто, экономически выгодно и износостойко - основные достоинства такого получения электричества.
- Кремний для зажигалок используется уже очень давно. Еще в древности люди использовали кремень для получения искры при розжиге огня. Этот принцип заложен в основу производства зажигалок различного рода. Сегодня встречаются виды, в которых кремень заменен на сплав определенного состава, дающий еще более быстрый результат (искрение).
- Электроника и солнечная энергетика.
- Изготовление зеркалец в газовых лазерных устройствах.
Таким образом, чистый кремний имеет массу преимущественных и особенных свойств, позволяющих использовать его для создания важных и нужных продуктов.
Применение соединений кремния
Помимо простого вещества, используются и различные соединения кремния, причем очень широко. Существует целая отрасль промышленности, которая называется силикатной. Именно она основана на использовании различных веществ, в состав которых входит этот удивительный элемент. Какие это соединения и что из них производят?
- Кварц, или речной песок - SiO 2 . Используется для изготовления таких строительных и декоративных материалов, как цемент и стекло. Где используются эти материалы, всем известно. Ни одно строительство не обходится без данных компонентов, что подтверждает значимость соединений кремния.
- Силикатная керамика, в которую входят такие материалы, как фаянс, фарфор, кирпич и продукты на их основе. Данные компоненты используются в медицине, при изготовлении посуды, декоративных украшений, предметов быта, в строительстве и прочих бытовых областях деятельности человека.
- - силиконы, силикагели, силиконовые масла.
- Силикатный клей - используется как канцелярский, в пиротехнике и строительстве.
Кремний, цена на который варьирует на мировом рынке, но не пересекает сверху вниз отметку в 100 рублей РФ за килограмм (за кристаллический), является востребованным и ценным веществом. Естественно, что и соединения этого элемента так же широко распространены и применимы.

Биологическая роль кремния
С точки зрения значимости для организма кремний немаловажен. Его содержание и распределение по тканям таково:
- 0,002 % - мышечная;
- 0,000017 % - костная;
- кровь - 3,9 мг/л.
Каждый день внутрь должно попадать около одного грамма кремния, иначе начнут развиваться заболевания. Смертельно опасных среди них нет, однако длительное кремниевое голодание приводит к:
- выпадению волос;
- появлению угревой сыпи и прыщей;
- хрупкости и ломкости костей;
- легкой проницаемости капилляров;
- усталости и головным болям;
- появлению многочисленных синяков и кровоподтеков.
Для растений кремний - важный микроэлемент, необходимый для нормального роста и развития. Опыты на животных показали, что лучше растут те особи, которые ежедневно потребляют достаточное количество кремния.